



| [jp] | top page | members | research | publications | class | lab |
research>>projects
(1)細胞のシステム統合工学1. マイクロ流体デバイスによる生命システム工学生体内の細胞は周囲の三次元環境とさまざま相互作用を行ないながら組織・臓器として機能している。多数の細胞が機能的に組み合わさることによって組織化するためのメカニズムは要素還元論に基づく分子生物学的な手法では理解することが難しく、再構成論的アプローチが必要となる。すわなち、細胞の配置、増殖因子の拡散・対流などを制御した環境を構築し、その中で細胞がどのように組織化していくかを調べることが必要となる。マイクロ流体システムはこのような微小細胞環境を制御するために有効なツールであり、多細胞の組織化を顕微鏡下でモニタリングすることが可能である。私たちは肝組織・毛細血管・胆管などの組織を生体外で再生させ、マイクロ流体システムを用いてこれらの細胞組織の相互作用を調べている。このテーマは、米国MITのProf. Kamm、韓国Korea UniversityのProf. Chungとの共同研究である。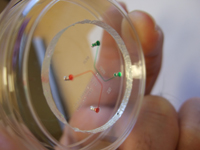
マイクロ流体システム 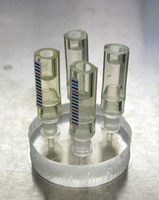
マイクロ流体システムによる培養環境の動的制御 
マイクロスケールでの拡散現象 2. 肝臓再生のシステムデザイン工学肝臓の細胞は、体内では極めて増殖が旺盛で再生する臓器として知られているが、肝細胞を体外に出してしまうと増殖しないという事が定説になっていた。ところが、札幌医科大学の三高俊広教授が肝臓内に前駆細胞と思われる増殖が旺盛な細胞が存在することを発見し、小型肝細胞と名付けた。小型肝細胞は体外でも著しく増殖するが、特に注目できる点は、小型肝細胞コロニー内に、実際の肝臓に存在する毛細胆管のネットワークが形成された事である。さらに毛細胆管のネットワークは、2次元的にも3次元的にも形成させることができ、小型肝細胞は肝臓再生のテクノロジーに有用であることが分かった。このテーマは、札幌医科大学の三高俊広教授、慶應義塾大学名誉教授池田満里子博士(細胞生物学)との共同研究である。詳細発表資料 [PDF] 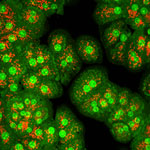
初代培養ラット肝細胞 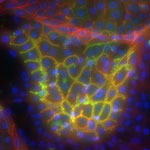
小型肝細胞が再生した毛細胆管の可視化 3. 管腔形成のバイオエンジニアリング組織再生を実現させるためには、再構築された細胞の集合体だけでは不十分である。即ち、細胞から分泌される有用物質を送り込む管や、細胞に酸素や栄養を与える血管網がないと細胞集合体が生存することが出来ない。そこで、小型肝細胞コロニー内に形成された毛細胆管と連結する胆管形成が必要となる。実際の肝臓の胆管上皮細胞を分離して、巧みな分化誘導を行うと、内径が数10 μmという比較的大きな胆管を体外で再生することに成功した。管腔形成を実現させるためには、細胞のもつ自己組織性を生体外で誘導するトリガーが必要で、発生生物学の知見が極めて重要となる。このテーマは、札幌医科大学の三高俊広教授、慶應義塾大学名誉教授池田満里子博士(細胞生物学)との共同研究である。詳細発表資料 [PDF] 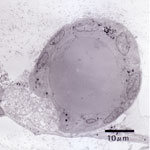
ラット胆管上皮細胞による胆管の再生1 透過型電子顕微鏡写真 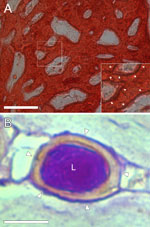
ラット胆管上皮細胞による胆管の再生2 GGT染色による内腔面の可視化 ラット胆管上皮細胞による胆管の再生3 再生された基底膜構造 4. 三次元毛細血管ネットワークの再生工学臓器機能に必要な管腔形成が実現できると、全ての細胞に酸素と栄養を与える血管網形成を実現させることが必要となる。血管網形成は、臓器再生で重要だが困難なテーマで、世界中の研究者が頭を悩ませている。最近、米国MITのLanger教授(臓器再生では最も先端的)のグループは、筋肉細胞の集合体に血管網を形成させることに成功している。そこで、当研究室では、血管網形成のテクノロジーを独立に開発している。これまでの知見として、血管内皮細胞を培養した表面にせん断応力の力学的な刺激を与えると、毛細血管網のようなネットワークの形成が促進されることが得られている。さらに、わざと低酸素状態にすると返って血管ネットワークの形成が促進されることも明らかになっており、血管網形成の基盤的研究を積み重ねている。詳細発表資料 [PDF] 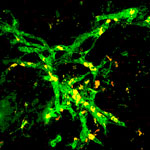
生体外における毛細血管ネットワークの再生1 共焦点レーザー顕微鏡画像 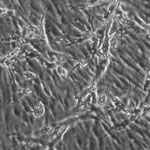
生体外における毛細血管ネットワークの再生2 位相差顕微鏡画像 (2)バイオメディカル流体力学 1. 人工血小板のナノバイオメカニクス血小板は血液中に含まれる細胞で、血管が切れた時に、凝集して止血作用をするという重要な役割を演じている。体内で血小板が減少する場合は、血小板輸血を行うが、最近医療現場で血小板輸血が増えてきたため、血小板が不足し、人工血小板の必要性が高まっている。そこで、国内では本塾医学部の池田康夫教授を中心に、人工血小板の開発が進められている。人工血小板の開発で重要な問題の一つは、如何に凝集現象を人工物が再現できているかである。そこで、実際の血小板の粘着・凝集を引き起こすレセプター(血管内表面に粘着する)を人工粒子表面に被覆し、モデル微小血管内での凝集現象を可視化して、粘着・凝集の評価を行っている。さらに、レセプターとリガンドとの結合によって生じる粘着力を直接原子間力顕微鏡で測定し、分子レベルの力学的特性を計測している。分子レベルの力学的な性質は、先端的なテーマで現在世界的に注目されている。このテーマは、人工血小板粒子を合成している早稲田大学理工学部武岡真司教授と共同研究である。詳細発表資料 [PDF] 
vWF A1 (Emsley et al., 1998) 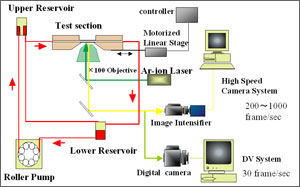
人工血小板粒子挙動解析の実験系 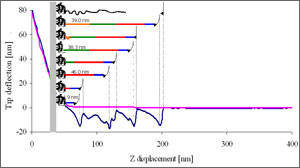
vWFとGPIbとの相互作用におけるAFMフォースカーブ 2. 脳内神経活動を支える血流と酸素輸送脳は体全体で使う酸素の20%も消費するという代謝が旺盛な臓器であるが、酸素不足に弱く、神経細胞への酸素輸送には謎に包まれている部分が多い。そこで、脳内の酸素環境を先端が10 μm以内の微小酸素電極により測定し、脳内血流からどのように酸素が供給されているかを調べている。その結果、脳内の微小血管網が巧みな分布をしており、神経細胞の局所的な活動により脳内酸素分圧が時空間的に変動している事が明らかになってきた。血流から脳組織への酸素輸送は、対流物質輸送として扱えるため、流体力学を基盤とする工学的なアプローチが有効で、今後脳科学分野に重要な知見を提供できる可能性が多い。このテーマは、日立製作所基礎研究所との共同研究である。詳細発表資料 [PDF] 
ラット脳内毛細血管ネットワークの可視化 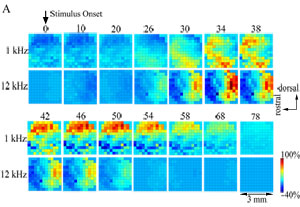
脳活動のカラーマッピング 3. 脳動脈瘤の血行力学と低侵襲診断治療のバイオエンジニアリング脳動脈に生じる瘤(血管のこぶ)は、脳ドックなどでよく発見されるが、医学界で信頼性の高い雑誌に、脳動脈瘤で破裂する例は少ないことが報告され、破裂する可能性のある脳動脈瘤を識別する診断基準が必要となっている。そこで、我々は、瘤内の血流構造が破裂との相関があるという仮説の基で、実際の患者さんのCT画像から3次元形態を再構築して、瘤内流れの解析を行い、診断基準の確立を目指している。さらに、破裂する可能性のある脳動脈瘤に関しては、低侵襲治療として有望視されているステント(血管内に留置する網目状の管)治療など、新しい治療を実現させるための血流解析を行っている。このテーマは、米国カリフォルニア大学ロサンジェルス校(UCLA)医学部Vinuela教授らのグループとの共同研究である。詳細発表資料 [PDF] 
脳血管と脳動脈瘤 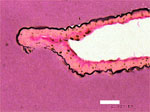
ラットに脳動脈瘤を誘発した脳血管組織増像 弾性板の断片化 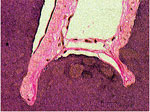
ラットに脳動脈瘤を誘発した脳血管組織増像 弾性板の断裂 4. 血管内治療に向けたステントのデザイン脳動脈瘤の治療では、瘤への血流を遮断することで血栓形成を促進させ破裂を防ぐことを目的とする。これまでその治療法としてクリッピングなどの開頭手術が行われてきたが、手術侵襲の問題などから、最近はカテーテルなどを用いた血管内治療が期待されている。 ステント治療は脳動脈瘤の血管内治療で近年最も注目されている。脳血管ステントには、頭蓋内の屈曲した血管形状に適応させるため、曲げ剛性などの力学的柔軟性が求められる。本研究室では、有限要素法による構造解析や、ステントサンプルの作成、力学特性測定や流体実験を行い、脳血管治療に有効なステントのデザインの実現を目指している。このテーマは、米国カリフォルニア大学ロサンジェルス校(UCLA)医学部Vinuela教授らのグループとの共同研究である。詳細発表資料 [PDF] 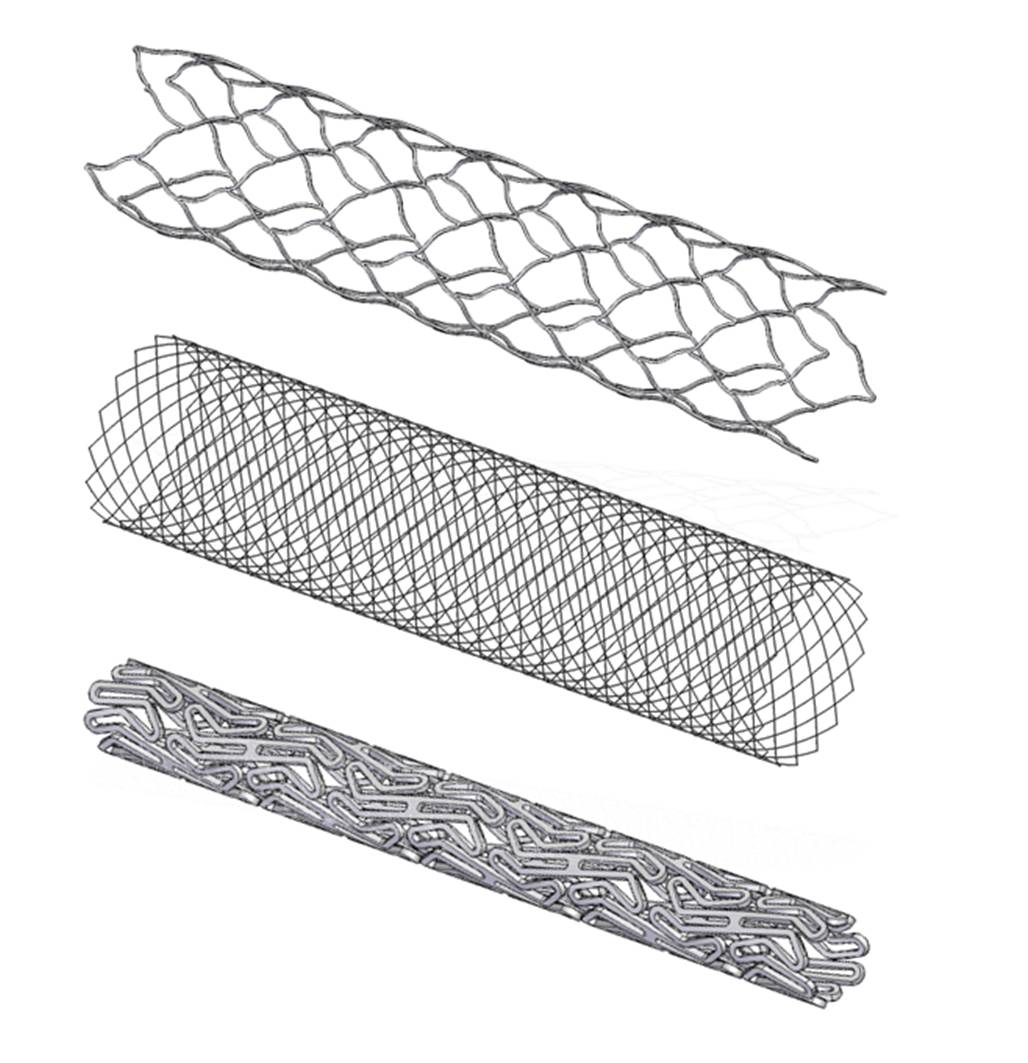
ステントの3DCADモデル 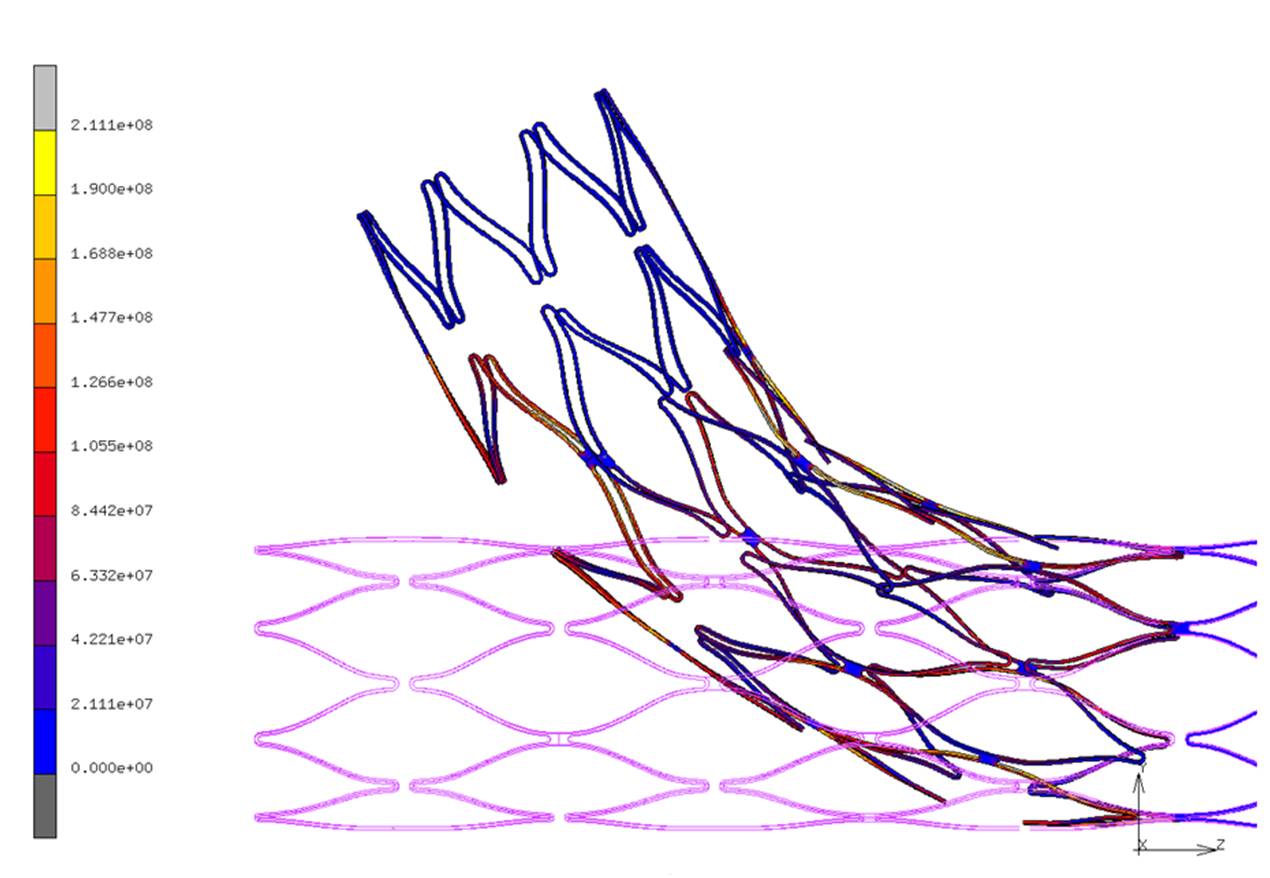
ステントの有限要素法による構造解析結果 5. 腫瘍血管内血流の制御がん治療で有望視されている治療法の一つにがん細胞に栄養を送る腫瘍血流を阻害して、兵糧攻めにする方法がある。さらに薬を病変部位のみに供給するというDrug Delivery System (DDS)も多くの医学者がその効果を期待しているが、いずれも腫瘍血管内血流を如何に制御するかが大きな課題となっている。そこで、マウスの背中の皮膚の血流を可視化する方法(Dorsal Skinfold Chamber)や乳腺の微小血管網を可視化する方法によって、腫瘍血管内血流を測定する方法を開発し、血流制御を中心にしたがん治療への応用を模索している。このテーマは、国立保健医療科学院牛山明博士、及び安村和彦博士との共同研究である。詳細発表資料 [PDF] 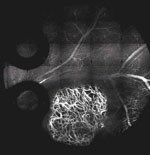
Dorsal Skinfold Chamberにおける腫瘍血管画像 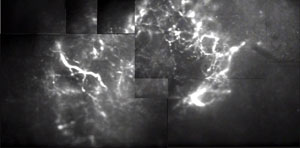
腫瘍血管画像の拡大図 |